Talidomid
Organiczny związek chemiczny zbudowany z reszty ftalimidowej i glutarimidowej. Wprowadzony do leczenia w 1958 roku jako lek przeciwdrgawkowy. Wkrótce talidomid stał się popularnym lekiem przeciwwymiotnym, który skutecznie hamował mdłości kobiet ciężarnych, obniżał ciśnienie krwi i znosił migrenowe bóle głowy. Już na początku lat 60 pojawiły się doniesienia o prawdopodobnej korelacji pomiędzy przyjmowaniem talidomidu a wadami rozwojowymi dzieci. W kolejnych latach efekty talidomidu zostały potwierdzone i lek uznano za toksyczny. Na wiele lat został wycofany z użycia i przez wiele lat był przykładem zagrożeń jakie niesie ze sobą rozwój farmaceutyczny. Talidomid przeżywa jednak swój renesans na nowo dzięki wprowadzeniu go do terapii przeciwnowotworowej oraz jako lek przeciwzapalny immunomodulacyjny. Od 1998 roku jest oficjalnie zarejestrowanym lekiem do leczenia zmian skórnych towarzyszących trądowi, atopowego zapalenia jamy ustnej, choroby Behceta, skórnej postaci tocznia rumieniowatego, choroby przeszczepowo-odrzuceniowej, wyniszczaniu w przebiegu AIDS, sarkoidozie, świądzie.
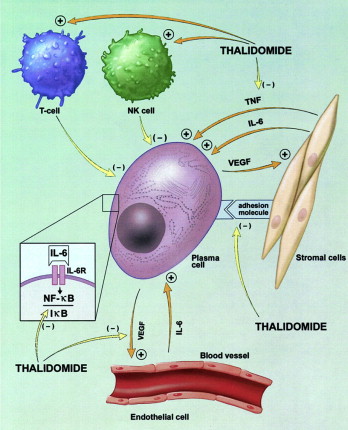
Dokładny mechanizm działania talidomidu nie został do końca jeszcze opisany. Wiadomo już, iż talidomid hamuje chemotaksję limfocytów i leukocytów wielojądrzastych, zmniejsza ekspresję cząsteczek adhezyjnych ICAM-1, hamuje prezentację antygenów przez układ MHC klasy II. Talidomid jest antagonistą działania prostaglandyn, serotoniny, histaminy, acetylocholiny, glikokortykosteroidów, hamuje także produkcję ROS. Właściwości immunomodulacyjne talidomidu są efektem obniżenia ilości limfocytów Th pomocniczych CD4 co zmienia profil wydzielanych cytokin biorących udział w reakcjach zapalnych. Wykazano m.in., iż talidomid zmniejsza wydzielanie TNFalfa, IL-5 nie zmieniając jednocześnie nasilenia syntezy IL-1, IL-6, GM-CSF. Hamowanie syntezy TNFalfa odbywa się na poziomie transkrypcji genu, poprzez skrócenie okresu półtrwania mRNA. Stymulujące działanie talidomidu obserwuje się natomiast w kierunku wydzielania IL-2, które wykazują działanie antyproliferacyjne i przeciwnowotworowe. Stymulacja IL-8 z kolei odpowiada za migrację i proliferację keratynocytów i tym samym przyspiesza regenerację uszkodzeń skóry i naskórka. Ważnym efektem działania talidomidu jest ograniczanie angiogenezy poprzez obniżenie poziomu VEGF i bFGF. Dzięki temu talidomid hamuje neowaskularyzację nowotworów: szpiczaka plazmocytowego, czerniaka, glejaka, raka prostaty, nerki, gruczołu piersiowego i jajnika. Schematyczna ilustracja efektów oddziaływania talidomidu jest przedstawiona na rysunku 1.
Piśmiennictwo: