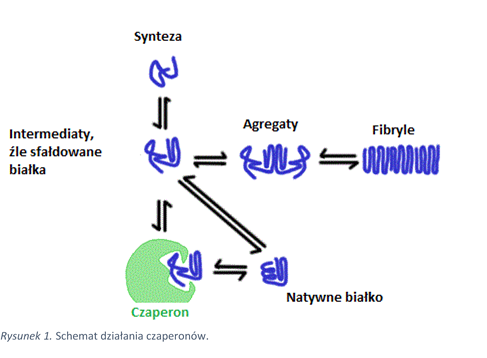
Czaperony (białka opiekuńcze)
Nazwa tych białek pochodzi od angielskiego słowa chaperone czyli opiekun. Są molekułami powszechnie występującymi w organizmach żywych, zarówno w bakteriach jak i u ludzi. W komórce są one w wysokich stężeniach. Są to białka, które odpowiadają za poprawne zwijanie się innych białek w warunkach fizjologicznych jak i w warunkach stresu. Mają zdolność rozpoznawania niesfałdowanych cząsteczek. Zapobiega to powstawaniu błędnych struktur białkowych oraz tworzeniu się agregatów. Trzeba jednak zaznaczyć, że czaperony nie niosą ze sobą informacji o sposobie fałdowania się białka, tylko zapobiegają powstaniu błędnych interakcji. Białka opiekuńcze można znaleźć we wszystkich kompartmentach komórki, gdzie obserwuje się zwijanie czy zmiany konformacyjne. Czaperony to duża grupa białek, która podzielona jest na klasy na podstawie ich masy molekularnej (Tabela 1). Między klasami białek opiekuńczych występują nieraz znaczne różnice. Mimo to można wyróżnić kilka cech wspólnych. Najbardziej znanymi czaperonami są: GroEL (E. coli), a także białka szoku cieplnego (ang. Heat shock proteins) Hsp70 czy Hsp90.
| Klasa | Struktura | ATP | Przykłady | Ko-czaperon | Funkcja (przykłady) | |
|---|---|---|---|---|---|---|
| Prokarioty | Eukarioty | |||||
| Hsp100 | 6-7 podjednostek | + | ClpB | usuwanie agregatów | ||
| ClpA | proteoliza | |||||
| Hsp104 | termotolerancja, usuwanie agregatów | |||||
| Hsp90 | dimer | + | HtpG | tolerancja na esktramalny stres komórkowy | ||
| Hsp90 | Hop,p23, CDC37 | tolerancja na stres, kontrola fałdowania oraz aktywności receptorów hormonów steridowych, kinaz białkowych itp. | ||||
| Hsp70 | monomer | + | DnaK | GnaJ, GrpE | fałdowanie białek de novo, zapobieganie agregacji zdenaturowanych białek, solubilizacja agregatów | |
| Hsp70, Hsc70 | Hsp40, Bag1, Hip, Chip, Hop, HspBP1 | fałdowanie białek de novo, zapobieganie agregacji zdenaturowanych białek, solubilizacja agregatów | ||||
| Hsp60 | 14,16 podjednostek | + | GroEL | GroES | fałdowanie białek de novo, zapobieganie agregacji zdenaturowanych białek | |
| CTT/TRiC | prefoldyna | fałdowanie de novo aktyny i tubuliny | ||||
| sHsp | 8-24 podjednostek | IbpA,IbpB | zapobieganie agregacji zdenaturowanych białek, wiązanie się do ciałek inkluzyjnych | |||
| Hsp25 | zapobieganie agregacji zdenaturowanych białek, składnik soczewek kręgowców | |||||
| Trigger factor | monomer | Trigger factor | potencjalnie funkcja w fałdowaniu białek związana z rybosomami | |||
| NAC | heterodimer | NAC | potencjalnie funkcja w fałdowaniu białek związana z rybosomami | |||
| SecB | tetramer | SecB | sekrecja białek | |||
Podstawową funkcją wszystkich czaperonów jest wspomaganie prawidłowego fałdowania białka. Zsyntetyzowane peptydy mogą eksponować hydrofobowe powierzchnie, które silnie promują agregację. Czaperony, wiążąc się do tych części niesfałdowanego, lub nawet do częściowo sfałdowanego białka (Rys.1) zapobiegają agregacji. Te niespecyficzne oddziaływania powodują, że czaperony wiążą się do wielu różnych peptydów. Należy jednak zauważyć, że jeśli białko nie eksponuje już części hydrofobowych, nie jest już dłużej substratem dla białka opiekuńczego. Co więcej czaperony mają możliwość zmiany konformacji białek, w których występują nienatywne wiązania, poprzez rozfałdowywanie aktualnej struktury peptydów. W wielu przypadkach, aby białko opiekuńcze oddysocjowało od proteiny, potrzebna jest energia pochodząca z hydrolizy ATP. Powoduje to zmianę konformacji czaperonu o wysokim powinowactwie do substratu na konformację o niskim powinowactwie i w efekcie końcowym jego dysocjację.
Literatura
- Priya S., Sharma S.K., Goloubinoff P. Molecular chaperones as enzymes that catalytically unfold misfolded peptides. FEBS Letters 2013, http://dx.doi.org/10.1016/j.febslet.2013.05.014
- Mogk A., Mayer M.P., Deuereling E. Mechanism of protein folding: Molecular Chaperones and their application in biotechnology. ChemBioChem 3 2002, 9:80-7-814.
- Walter S., Buchner J. Molecular Chaperones- Cellular machines for protein folding. Angewandte Chemie International Edition 2002, 41: 1098-1113.
- Buchner J. Supervising the fold: functional principles of molecular chaperones. The FASEB Journal 1996, 10:10-19.