(→Kinaza JAK2) |
(→Kinaza JAK2) |
||
| Linia 5: | Linia 5: | ||
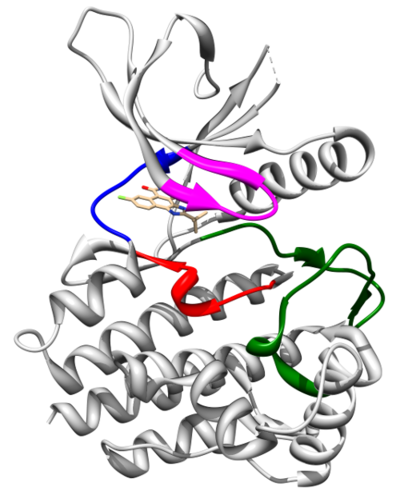
Pierwsza poznana struktura domeny kinazowej JAK2 to struktura krystalograficzna kompleksu tej domeny z inhibitorem CMP6 (Lucet et al. 2006). Ma ona typową dla kinaz dwupłatową budowę z płatem N-terminalnym (aminokwasy 840-931) oraz C-terminalnym (932-1132). Pierwszy płat jest złożony z pięciu antyrównoległych wstążek beta i jednej helisy alfa (αC). Drugi natomiast jest zbudowany z ośmiu helis alfa (αD-αK) i trzech par antyrównoległych wstążek beta (β7-β8, β6-β9, β10-β11). Centrum aktywne, wraz z miejscem wiązania cząsteczki ATP, znajduje się w kieszeni pomiędzy płatami, które połączone są tzw. regionem zawiasowym. Pętla aktywacyjna również (aminokwasy 994-1023) uczestniczy w wiązanu substratów reakcji fosforylacji: cząsteczki ATP oraz białka. Autofosforylacja tyrozyny 1007 oraz 1008 działa jak molekularny przełącznik aktywności fosforylacyjnej kinazy JAK2. W wyniku autofosforylacji Tyr1007 oraz Tyr1008 dochodzi do otwarcia pętli aktywacyjnej i przesunięcia motywu DFG (aminokwasy 994-996), oddziałującego z jonami Mg<sup>2+</sup>, w pobliże centrum aktywnego. Autofosforylacja umożliwia ponadto wiązanie wielu białek regulatorowych, jak SOCS czy PTP. Pętla insercyjna (aminokwasy 1056-1078), charakterystyczna dla wszystkich domen kinazowych JAK, przypuszczalnie zaangażowana jest w regulację fosforylacji tych białek. | Pierwsza poznana struktura domeny kinazowej JAK2 to struktura krystalograficzna kompleksu tej domeny z inhibitorem CMP6 (Lucet et al. 2006). Ma ona typową dla kinaz dwupłatową budowę z płatem N-terminalnym (aminokwasy 840-931) oraz C-terminalnym (932-1132). Pierwszy płat jest złożony z pięciu antyrównoległych wstążek beta i jednej helisy alfa (αC). Drugi natomiast jest zbudowany z ośmiu helis alfa (αD-αK) i trzech par antyrównoległych wstążek beta (β7-β8, β6-β9, β10-β11). Centrum aktywne, wraz z miejscem wiązania cząsteczki ATP, znajduje się w kieszeni pomiędzy płatami, które połączone są tzw. regionem zawiasowym. Pętla aktywacyjna również (aminokwasy 994-1023) uczestniczy w wiązanu substratów reakcji fosforylacji: cząsteczki ATP oraz białka. Autofosforylacja tyrozyny 1007 oraz 1008 działa jak molekularny przełącznik aktywności fosforylacyjnej kinazy JAK2. W wyniku autofosforylacji Tyr1007 oraz Tyr1008 dochodzi do otwarcia pętli aktywacyjnej i przesunięcia motywu DFG (aminokwasy 994-996), oddziałującego z jonami Mg<sup>2+</sup>, w pobliże centrum aktywnego. Autofosforylacja umożliwia ponadto wiązanie wielu białek regulatorowych, jak SOCS czy PTP. Pętla insercyjna (aminokwasy 1056-1078), charakterystyczna dla wszystkich domen kinazowych JAK, przypuszczalnie zaangażowana jest w regulację fosforylacji tych białek. | ||
| − | {|class="wikitable | + | {|class="wikitable center" style="text-align:center; font-size:75%; border:1px" |
|+ Tabela 1: Konserwowane elementy struktury domeny kinazowej JAK2 | |+ Tabela 1: Konserwowane elementy struktury domeny kinazowej JAK2 | ||
! fragment struktury | ! fragment struktury | ||
Wersja z 18:17, 12 maj 2014
Kinaza JAK2
Kinaza JAK2 należy do rodziny niereceptorowych tyrozynowych kinaz białkowych JAK. Kinaza ta jest częścią ścieżek sygnalnych JAK2/STAT3/5 (Signal Transducer and Activator of Transcription) i uczestniczy w transdukcji sygnałów zewnątrzkomórkowych za pośrednictwem cytokin, czynników wzrostu i hormonów. Ma typową dla białek JAK czterodomenową budowę - od C-końca można wyróżnić następujące domeny: JH1, JH2, SH2 oraz FERM. Domena JH1 (aminokwasy 835 do 1132, PubMed NM 004972) kinazy JAK2 jest typową dla komórek eukariotycznych domeną katalityczną o aktywności kinazy tyrozynowej (PTK - Protein Tyrosine Kinase). Spełnia ona trzy kluczowe role: wiązanie i pozycjonowanie donora reszty fosforanowej (ATP, GTP) w kompleksie z dwuwartościowymi kationami (Mg2+, Mn2+), wiązanie i pozycjonowanie substratu peptydowego, a także transfer γ-fosforanu na aminokwas akceptorowy.
Pierwsza poznana struktura domeny kinazowej JAK2 to struktura krystalograficzna kompleksu tej domeny z inhibitorem CMP6 (Lucet et al. 2006). Ma ona typową dla kinaz dwupłatową budowę z płatem N-terminalnym (aminokwasy 840-931) oraz C-terminalnym (932-1132). Pierwszy płat jest złożony z pięciu antyrównoległych wstążek beta i jednej helisy alfa (αC). Drugi natomiast jest zbudowany z ośmiu helis alfa (αD-αK) i trzech par antyrównoległych wstążek beta (β7-β8, β6-β9, β10-β11). Centrum aktywne, wraz z miejscem wiązania cząsteczki ATP, znajduje się w kieszeni pomiędzy płatami, które połączone są tzw. regionem zawiasowym. Pętla aktywacyjna również (aminokwasy 994-1023) uczestniczy w wiązanu substratów reakcji fosforylacji: cząsteczki ATP oraz białka. Autofosforylacja tyrozyny 1007 oraz 1008 działa jak molekularny przełącznik aktywności fosforylacyjnej kinazy JAK2. W wyniku autofosforylacji Tyr1007 oraz Tyr1008 dochodzi do otwarcia pętli aktywacyjnej i przesunięcia motywu DFG (aminokwasy 994-996), oddziałującego z jonami Mg2+, w pobliże centrum aktywnego. Autofosforylacja umożliwia ponadto wiązanie wielu białek regulatorowych, jak SOCS czy PTP. Pętla insercyjna (aminokwasy 1056-1078), charakterystyczna dla wszystkich domen kinazowych JAK, przypuszczalnie zaangażowana jest w regulację fosforylacji tych białek.
| fragment struktury | aminokwasy | struktura kompleksu domeny kinazowej JAK2 z inhibitorem CMP6 (kod PDB: 2B7A) |
|---|---|---|
| rejon zawiasowy | 929-935 (MEYLPYG) |
|
| pętla glicynowa | 856-861 (GKGNFG) | |
| pętla katalityczna (motyw PTK – Protein Tyrosine Kinase Active-site Signature) | 972-984 (YIHRDLATRNILV) | |
| pętla aktywacyjna (z motywami DFG (994-996) i APE (1022-1024) oraz autofosforylowaną parą tyrozyn Y1007/Y1008) | 994-1024 (DFGLTKVLPQDKEYY KVKEPGESPIFWYAPE) |