VEGF
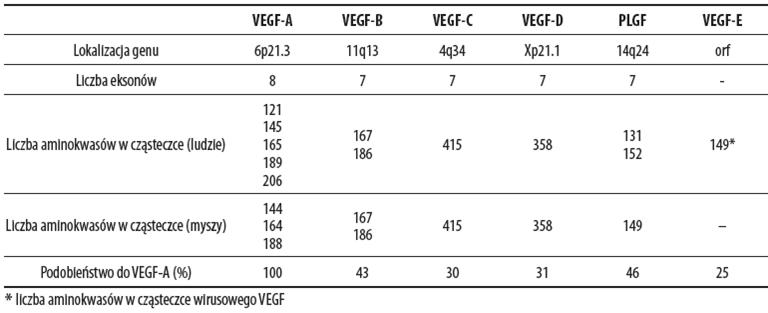
Do rodziny VEGF (z ang. vascular endothelial growth factor) należą VEGF-A, VEGF-B, -C, -D, PIGF (łożyskowy czynnik wzrostu), i VEGF-E (wirusowy homolog). Cechą wspólną tych cytokin jest obecność w cząsteczce fragmentu zawierającego sekwencję cystein, dzięki którym tworzone są mostki disiarczkowe i dimery. Poszczególne cytokiny są produktami różnych genów, mają odmienną strukturę i działanie biologiczne. Porównanie właściwości czynników VEGF zawiera Tabela 1.
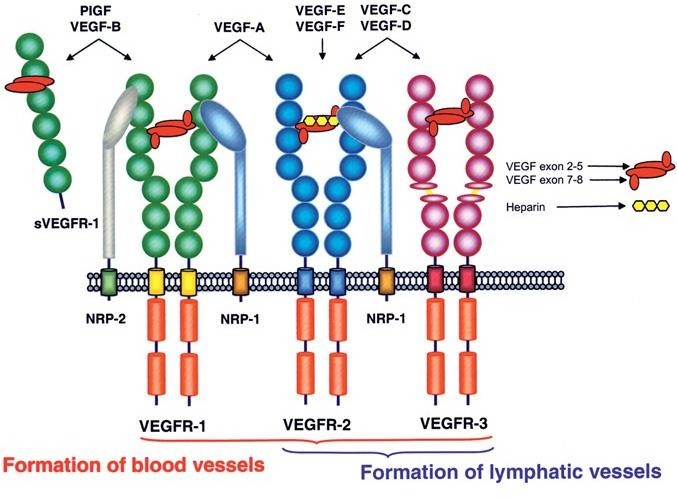
VEGF-A jest najlepiej poznanym przedstawicielem rodziny VEGF. W wyniku ekspresji genu zlokalizowanego na chromosomie 6 oraz alternatywnego składania powstają izoformy VEGF-A o różnej długości łańcucha polipeptydowego (121, 145, 165, 189 oraz 206 aa). Podstawowa funkcja biologiczna VEGF polega na indukcji budowy naczyń krwionośnych i zwiększania ich przepuszczalności. Nasilenie efektów biologicznych VEGF-A jest uzależnione od aktywnej izoformy czynnika i jej powinowactwa do heparyny. Synteza VEGF zachodzi w wielu typach komórek organizmu, m.in. komórkach mięśni gładkich naczyń, makrofagach, fibroblastach oraz komórkach śródbłonka. Inicjatorami syntezy VEGF jest hipoksja, oraz cytokiny: TNF-alfa, IL-1beta, czynniki wzrostu: bFGF, TGF, reaktywne formy tlenu oraz chelatory żelaza. Działanie VEGF jest modyfikowane przez czynniki wspomagające. Do czynników wspomagających należy neuropilina 1 i 2 (NRP-1, NRP-2), które pełnią funkcję koreceptorów. Neuropiliny są niezbędne dla prawidłowego przebiegu angiogenezy. Ich synteza zachodzi głównie w zakończeniach aksonów, komórkach śródbłonka naczyń krwionośnych oraz w komórkach nowotworowych. NRP-1 wzmacnia wiązanie VEGF165 do receptora VEGF2, podczas gdy NRP-2 wiąże VEGF-C i współdziała z VEGF-R3. Schematyczna ilustracja oddziaływania czynników VEGF na swoiste receptory oraz rola NRP-1 i NRP-2 przedstawiona jest na rysunku 1.
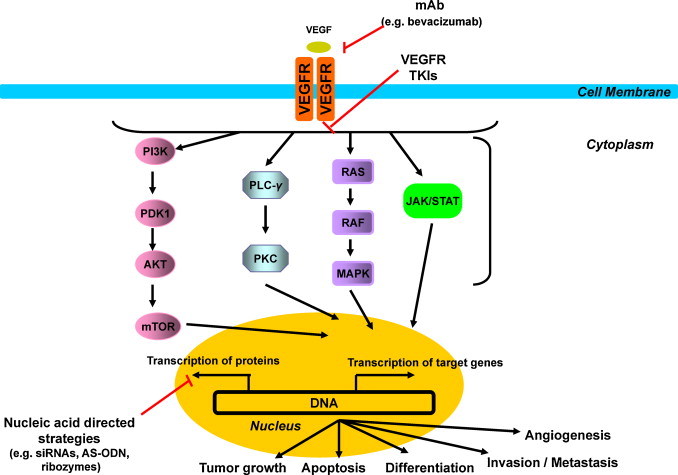
Interakcja cytokiny VEGF ze swoistym receptorem aktywuje w komórce kilka szlaków sygnałowych w zależności od rodzaju receptora VEGF-R. Najlepiej poznana droga sygnałowa została opisana dla VEGFR-2. Obecność VEGF indukuje autofosforylację białek receptora VEGFR-2, która umożliwia przyłączenie białek komórkowych Shc i Grb2. Cząsteczki te tworząc kompleks SOS-Ras, prowadzą do aktywacji kaskady Ras-Raf-MAP, która jest bezpośrednio odpowiedzialna za proliferację śródbłonka. Przyłączenie VEGF do VEGFR-2 prowadzi również do przyłączenia fosfolipazy C gamma, która odcina fragment fosfatydyloinozytolu od jego miejsca zakotwiczenia w lipidzie, uwalniając w ten sposób fosforan inozytolu (IP3). IP3 prowadzi z kolei do uwolnienia jonów Ca z puli jonów wewnątrzkomórkowych. Wraz z IP3 powstaje diacylglicerol (DAG), który pozostając w sąsiedztwie błony komórkowej odpowiada za aktywację kinaz PKC. Aktywacja PKC jest związana z migracją i przepuszczalnością naczyń. Badania wskazują, iż VEGF jest także aktywatorem dwóch kolejnych szlaków komórkowych: JAK/STAT oraz PI3-K/Akt/mTOR. Schematyczna ilustracja szlaków sygnałowych aktywowanych przez VEGF jest przedstawiona na rysunku 2.
Rola VEGF w procesie angiogenezy VEGF jest cytokiną kluczową dla rozwoju w okresie natalnym. Wydzielanie VEGF jest obserwowane już na etapie gastruli przez komórki mezodermy i endodermy. Ważnym czynnikiem regulującym jest obecność receptora VEGFR-2. Brak ekspresji receptora koreluje z brakiem tworzenia wysp krwiotwórczych i obumarciem zarodka. Aktywacja VEGFR-2 na powierzchni komórek endotelialnych stymuluje ich migrację i różnicowanie, natomiast aktywacja komórek mezodermalnych stymuluje różnicowanie w kierunku linii śródbłonkowej oraz komórek mięśni gładkich. Proces angiogenezy zachodzi również w okresie postnatalnym. Jest fizjologicznym zjawiskiem procesów regeneracji, przebiegu owulacji, menstruacji, wzrostu włosów, czy dojrzewania kości. Również w tych procesach dominującą rolę odgrywa VEGFR-2, którego aktywacja promuje różnicowanie progenitorowych komórek śródbłonka, ich podziały oraz degradację błony podstawnej umożliwiającej formowanie nowych naczyń.
Rola VEGF w procesie neurogenezy W układzie nerwowym VEGF, poza pierwotną funkcją stymulatora angiogenezy, może oddziaływać na różnego rodzaju komórki nerwowe, w tym macierzyste komórki neuralne. Obecność VEGF wykryto również w neuronach i komórkach glejowych. Wykazano m.in. iż VEGF oddziałuje na komórki Schwanna a także astrocyty. VEGF wytwarzany przez komórki wyściółki układu komorowego mózgu i rdzenia stymuluje proliferację prekursorów w strefie podkorowej i podziarnistej zakrętu zębatego i hipokampa. Pobudza także neurogenezę poprzez pobudzanie komórek śródbłonka do syntezy czynników neutroficznych.
Piśmiennictwo:
- www.phmd.pl/fulltxt.php?ICID=435712
- http://www.ncbi.nlm.nih.gov/pubmed/16728325
- http://www.ncbi.nlm.nih.gov/pubmed/12778165