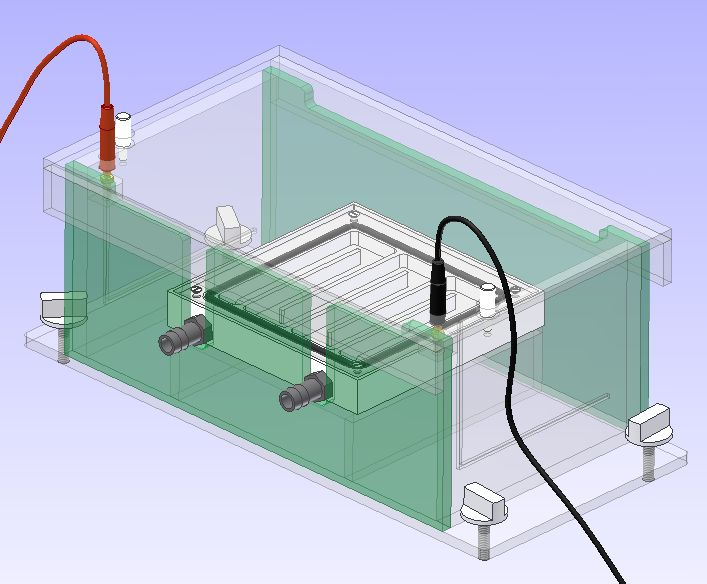
IEF
IEF, czyli izoelektryczne ogniskowanie (skrót z ang. IEF – isoelectric focusing) jest rodzajem elektroforezy, która jest jednocześnie pierwszym etapem elektroforezy dwukierunkowej. Wartość pH buforu w metodzie IEF nie jest stała. Przechodzi ona od najwyższej przy katodzie do wartości najniższej przy anodzie. Liniowy gradient pH tworzą amfoliny (kondensat poliaminy z kwasem akryloaminowym), które mają szeroki zakres środowiska pH, od 3 do 10 (gradient ten cechuje się wysoką stabilnością). W IEF separacja molekuł substancji odbywa się ze względu na jej wartość pI. Wartość ta to takie pH, w którym wypadkowy ładunek makrocząsteczki równy jest 0. Na elektrycznie obojętną substancję nie działają siły pola, zatem pozostaje ona w spoczynku. Jeżeli molekuła znajduje się w środowisku o wyższym pH, w wyniku utraty protonu staje się ujemnie naładowaną molekułą, która będzie się przemieszczać w kierunku dodatniej anody. Odwrotnie gdy molekuła znajdzie się w środowisku o niższym pH.
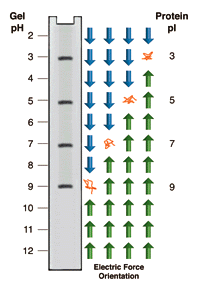
Technika ta charakteryzuje się bardzo wysoką zdolnością rozdzielczą, Różnica wartości pH równa zaledwie 0,02 jest wystarczająca do odseparowania cząsteczek.
Przykładem aparatu wykorzystywanym do izoogniskowania jest ISOGEL firmy Kucharczyk TE. Aparat jest zintegrowany z systemem chołodząco-grzejmym LcooL (Kucharczyk TE ®), który utrzymuje stałą, zadaną temperaturę na płytce podczas całego procesu. Ciepło odprowadzane jest poprzez opływającą spód płytki ciecz. Po przygotowaniu żelu poliakrylamidowego wykonuje się preogniskowanie a w następnie wykonuje się ogniskowanie interesujących nas próbek. Efektem końcowym są precypitaty wytrąconych białek, które po wybarwieniu i zeskanowaniu możemy analizować.
Literatura