| Linia 1: | Linia 1: | ||
{{tooltip|base|ooo}} | {{tooltip|base|ooo}} | ||
| − | <tooltip text="body text" x= | + | <tooltip text="body text" x=0 y=0>tooltip text</tooltip> |
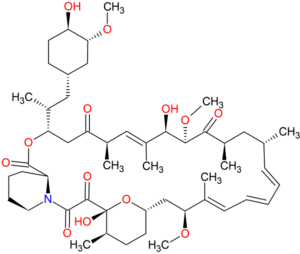
[[Image:Rapamycyna-Rysunek1.png|thumb|300px|Struktura chemiczna rapamycyny]] | [[Image:Rapamycyna-Rysunek1.png|thumb|300px|Struktura chemiczna rapamycyny]] | ||
Wersja z 11:01, 10 cze 2014
base
<tooltip text="body text" x=0 y=0>tooltip text</tooltip>
Rapamycyna, znana również jako sirolimus, jest naturalnym laktonem makrocyklicznym, wyizolowanym z gleby na wyspie Wielkanocnej w latach 70-tych ubiegłego stulecia jako związek o aktywności przeciwgrzybiczej.[1] Syntetyzowany jest przez mikroorganizm o nazwie Streptomyces hygroscopicus. Rapamycyna jest inhibitorem kinazy mTOR (mechanistic target of rapamycin).[2][3] do najważniejszych właściwości biologicznych tego inhibitora należą:
- przeciwnowotworowe, hamowanie proliferacji i wzrostu komórek eukariotycznych (własności ),
- immunosupresyjne poprzez hamowanie aktywacji i proliferacji limfocytów T (aktywacja limfocytów T zachodzi w odpowiedzi na stymulację antygenową i cytokinową),
- hamowanie produkcji przeciwciał,
- przeciwgrzybicze,
- hamowanie produkcji cytokin poprzez selektywne blokowanie aktywacji transkrypcyjnej ich genów
Właściwości bioaktywne rapamycyne są zalezne od wiązania tego antybiotyku przez immunofiliny.
Rapamycyna tworzy kompleks z białkiem FKBP12 (FK506-binding protein 12) oraz domeną FRB (FKBP12–rapamycin binding) kinazy mTOR.[4][5][6] Białka te oddziałują głównie z cząsteczką rapamycyny, natomiast bezpośrednie oddziaływanie FKBP12-mTOR ma minimalny wpływ na tworzenie kompleksu. Antybiotyk ten umożliwia zatem dimeryzację białka FKBP12 oraz domeny FRB. Kompleks rapamycyna–FKBP12 jest allosterycznym inhibitorem TORC1. Mechanizm inhibicji może być przynajmniej częściowo wyjaśniony poprzez blokowanie dostępu substratów do centrum aktywnego kinazy mTOR.[7][8][9][10] Odległość pomiędzy FKBP12 oraz mLST8 może zmniejszać się zaledwie do 8 Å, zamykając i tak wąską szczelinę prowadzącą do centrum aktywnego kinazy mTOR. Rapamycyna hamuje TORC1 w różnym stopniu w zależności od substratów reakcji fosforylacji (np. S6K1 vs. 4E-BP1), a także fosforylowanych aminokwasów.
Analogi chemiczne rapamycyny nazywane są rapalogami. Obecnie rapalogi znajdują się w fazie testów klinicznych jako potencjalne leki przeciwko chorobom nowotworowym, autoimmunologicznym (jak np. reumatoidalne zapalenie stawów), a także w transplantologii czy też leczeniu restenozy wieńcowej.
| rapalog | badania kliniczne | wskazanie terapeutyczne | nazwa leku | firma (rok zatwierdzenia) |
|---|---|---|---|---|
| rapamycyna (sirolimus) | - | transplantologia nerki | Sirolimus | Zydus Pharmaceuticals (2014) |
| rapamycyna (sirolimus) | - | transplantologia nerki | Rapamune | PF PRISM CV (2000) |
| temsirolimus | - | rak nerkowokomórkowy w zaawansowanym stadium | Torisel | PF PRISM CV (2007) |
| () |
Najważniejsze skutki uboczne stosowania rapalogów to:
- podwyższone ryzyko nowotworów, głównie chłoniaków oraz nowotworów skóry
- podwyższone ryzyko infekcji, w tym zagrażających życiu pacjenta.
Są one konsekwencją osłabienia działania układu immunologicznego przez rapamycynę oraz jej analogi. Nie zaleca się podawania leku u chorych po przeszczepie płuc lub wątroby.
Literatura
- ↑ Vézina C, Kudelski A, Sehgal SN. Rapamycin (AY-22,989), a new antifungal antibiotic. I. Taxonomy of the producing streptomycete and isolation of the active principle. The Journal of Antibiotics. 1975;28(10):721-6.
- ↑ Heitman J, Movva NR, Hall MN. Targets for cell cycle arrest by the immunosuppressant rapamycin in yeast. Science. 1991;253(5022):905–9.
- ↑ Zheng XF, Florentino D, Chen J, Crabtree GR, Schreiber SL. TOR kinase domains are required for two distinct functions, only one of which is inhibited by rapamycin. Cell. 1995;82:121-130.
- ↑ Brown EJ, Albers MW, Shin TB, Ichikawa K, Keith CT, Lane WS, Schreiber SL. A mammalian protein targeted by G1-arresting rapamycin-receptor complex. Nature. 1994;369(6483):756-8.
- ↑ Sabatini DM, Erdjument-Bromage H, Lui M, Tempst P, Snyder SH. RAFT1: a mammalian protein that binds to FKBP12 in a rapamycin-dependent fashion and is homologous to yeast TORs. Cell. 1994;78(1):35-43.
- ↑ Sabers CJ, Martin MM, Brunn GJ, Williams JM, Dumont FJ, Wiederrecht G, Abraham RT. Isolation of a protein target of the FKBP12-rapamycin complex in mammalian cells. The Journal of Biological Chemistry. 1995;270(2):815-22.
- ↑ Choi J, Chen J, Schreiber SL, Clardy J. Structure of the FKBP12-rapamycin complex interacting with the binding domain of human FRAP. Science. 1996;273(5272):239-42.
- ↑ Liang J, Choi J, Clardy J. Refined structure of the FKBP12-rapamycin-FRB ternary complex at 2.2 A resolution. Acta Crystallographica. Section D, Biological Crystallography. 1999;55(Pt 4):736-44.
- ↑ Choo AY, Blenis J. Not all substrates are treated equally: implications for mTOR, rapamycin-resistance and cancer therapy. Cell Cycle. 2009;8(4):567-72.
- ↑ Yang H, Rudge DG, Koos JD, Vaidialingam B, Yang HJ, Pavletich NP. mTOR kinase structure, mechanism and regulation. Nature. 2013;497(7448):217-23.